Содержание:
- 1. Основные положения клеточной теории
- 2. Содержание и роль химических элементов в клетке
- 3. Вода и ее роль в организме
- 4. Органические вещества клетки. Общая характеристика
- 5. Ферменты (энзимы)
- 6. Липиды
- 7. Углеводы (сахариды) (оболочка)
- 8. Пигменты
Основные положения клеточной теории
Первое наблюдение клетки: Р. Гук (Англия, 1665 г.).
Клеточная теория — одна из важнейших биологических теорий, являющаяся обобщением огромного количества данных, согласно которой жизнь существует только в форме клеток и их совокупностей.
Впервые клеточную теорию предложил Г. Шванн (Германия, 1839 г.); ее дальнейшие разработки: Р. Вирхов (Германия, 1858 г.), И. Чистяков (Россия, 1874 г.), Э. Страсбургер (Польша, 1875 г.) и др.
♦ Основные положения современной клеточной теории:
■ клетка — элементарная (наименьшая) структурная, функциональная и генетическая единица всех живых организмов, способная к самообновлению, саморегуляции и самовоспроизведению;
■ клетки живых организмов сходны по строению, химическому составу и основным проявлениям жизнедеятельности;
■ размножение клеток происходит путем их деления; каждая новая клетка образуется в результате деления исходной (материнской) клетки;
■ клетки специализируются по функциям; структура и функции клеток взаимосвязаны. В многоклеточном организме клетки образуют ткани, из которых строятся органы, системы органов и весь организм, функционирующий как единое целое благодаря нервной и гуморальной регуляции.
Содержание и роль химических элементов в клетке
❖ Основные элементы: кислород О (примерно 62% массы клетки), углерод С (20%), водород Н (10%), азот N (3,5%); они входят в состав всех органических веществ.
❖ Макроэлементы — элементы с содержанием более 0,01% массы клетки: кальций, фосфор, сера, калий, натрий, магний, хлор.
| Элемент | Содержание в клетке, свойства и роль |
| Са (2,5%) | Входит в состав клеточной стенки растений, костной ткани, зубной эмали, известкового скелета животных; Са** усиливает работу сердца, участвует в процессах сокращения мышц и свертывания крови |
| Р (1,0%) | Входит в состав ДНК, РНК, АТФ, ряда ферментов, костной ткани, зубной эмали |
| S (0,25%) | Входит в состав важнейших аминокислот и белков |
| К (0,25%) | Входит в состав хлорофилла, зубов, костей и некоторых ферментов; повышает активность ферментов; К+ поддерживает разность потенциалов в клетке, участвует в передаче нервных импульсов, уменьшает силу сердечных сокращений |
| Na (0,10%) | Поддерживает нормальный ритм сердечной деятельности и щелочно-кислотное равновесие; Na+ участвует в передаче нервных импульсов |
| Mg (0,07% | Входит в состав хлорофилла, некоторых ферментов, костной ткани, зубной эмали, активизирует синтез ДНК |
❖ Микроэлементы — элементы с содержанием не более 0,01% массы клетки (Fe, Сu и др., см. таблицу), входящие в состав гормонов, витаминов, дыхательных ферментов. Недостаток любого из них вызывает серьезные нарушения в обмене веществ.
| Элемент | Содержание в клетке, свойства и роль |
| Fe | Входит в состав гемоглобина и миоглобина, многих ферментов, участвует в процессах дыхания и фотосинтеза |
| I | Входит в состав гормона щитовидной железы |
| F | Входит в состав зубной эмали и костной ткани |
| Cu | Входит в состав гормона поджелудочной железы, ферментов, необходимых для фотосинтеза, кроветворения, синтеза гемоглобина |
| Mn | Входит в состав ферментов, необходим для развития костей |
| Mo | Входит в состав некоторых ферментов, участвует в фиксации азота клубеньковыми бактериями |
| Co | Входит в состав витамина В|2, участвует в развитии эритроцитов и фиксации азота клубеньковыми бактериями |
| Zn | Входит в состав некоторых ферментов; необходим для синтеза фитогормонов |
| В | Влияет на процессы роста растений |
❖ Ультрамикроэлементы (Se, V, Ag, Au и др.) имеют концентрации менее 10-12%. Например, элементы Ag, Au входят в состав волос.
❖ Ионы Н2РO4, НPО42- необходимы для синтеза АТФ, эти же ионы и ионы С1—, НСO3 , SO4 ” и др. участвуют в поддержке pH клетки, активации ферментов и т.д.
Вода и ее роль в организме
❖ Основные свойства воды:
■ малые размеры молекул;
■ их полярность;
■ способность молекул соединяться друг с другом водородными связями;
■ высокие удельная теплоемкость и теплопроводность;
■ высокая удельная теплота парообразования;
■ высокое поверхностное натяжение.
— Регулярная проверка качества ссылок по более чем 100 показателям и ежедневный пересчет показателей качества проекта.
— Все известные форматы ссылок: арендные ссылки, вечные ссылки, публикации (упоминания, мнения, отзывы, статьи, пресс-релизы).
— SeoHammer покажет, где рост или падение, а также запросы, на которые нужно обратить внимание.
SeoHammer еще предоставляет технологию Буст, она ускоряет продвижение в десятки раз, а первые результаты появляются уже в течение первых 7 дней. Зарегистрироваться и Начать продвижение
❖ Основные функции воды в организме:
■ вода — универсальный растворитель для полярных веществ,
■ регулирует тепловой режим клетки,
■ выполняет транспортную функцию (обеспечивает поступление веществ в клетку, их передвижение в клетке и выделение из клетки),
■ выполняет метаболическую функцию (является средой для протекания всех биохимических реакций, сама участвует в реакции гидролиза и многих других реакциях, является источником кислорода и водорода при фотосинтезе и т.д.),
■ выполняет структурную функцию (обеспечивает упругость и тургор клеток, т.е. их напряженное состояние, обусловленное внутриклеточным давлением; у некоторых животных является гидростатическим скелетом),
■ регулирует осмотическое давление в клетке,
■ связанная вода образует сольватные оболочки вокруг белковых молекул, и др.
| Содержание воды в клетках | % |
| Мышечные клетки | 76 |
| Клетки эмбриона | 95 |
| Клетки нервной ткани | 85 |
| Клетки жировой ткани | 40 |
| Клетки костной ткани | 50 |
| Клетки зубной эмали | 10 |
| Связанная вода | 5 |
Органические вещества клетки. Общая характеристика
Биополимеры — высокомолекулярные (относительная молекулярная масса 103 — 10-4) органические соединения, молекулы которых состоят из большого числа повторяющихся звеньев мономеров.
Биополимеры составляют до 90% сухого вещества клетки.
♦Важнейшие классы органических соединений, составляющих молекулярную основу любой живой клетки:
■ белки,
■ липиды,
■ углеводы,
■ нуклеиновые кислоты.
(Свойства этих классов соединений рассмотрены ниже). В клетках растений преобладают углеводы, в клетках животных — белки.
❖ Аминокислоты — низкомолекулярные органические соединения,
содержащие одну или две карбоксильные (-СООН) и одну или две аминную (-NH2) группы (обладающие соответственно кислотными и щелочными свойствами), причем карбоксильная и аминная группы связаны с одним и тем же атомом углерода.
■ Аминокислоты — амфотерные соединения (проявляют свойства и кислот, и оснований).
❖Пептиды — это органические молекулы, образующиеся при взаимодействии аминогруппы одной аминокислоты с карбоксильной группой другой аминокислоты.
❖ Пептидная связь — связь -CO-NH-.
Белки — природные высокомолекулярные органические соединения (полипептиды), молекулы которых образованы аминокислотными остатками (в количестве от 50 до нескольких тысяч).
■ В состав белков входит только 20 видов аминокислот (из 150 видов, существующих в природе).
■ Белки составляют Ю-18% от общей массы клетки.
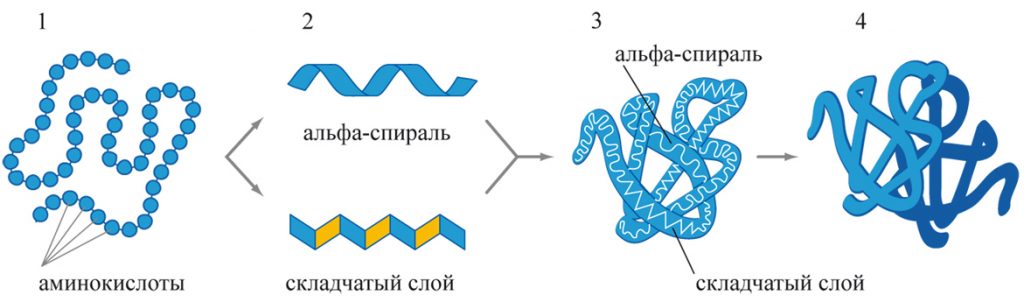
Уровни структурной организации белков:
■ первичная структура белка определяется последовательностью соединения аминокислот, закодированной в ДНК, и обусловлена пептидными связями;
■ вторичная структура (спираль) возникает из-за образования водородных связей между СО- и NH- -группами, расположенными на соседних витках (такую структуру имеют фибриноген, миозин, актин)
— Разгрузит мастера, специалиста или компанию;
— Позволит гибко управлять расписанием и загрузкой;
— Разошлет оповещения о новых услугах или акциях;
— Позволит принять оплату на карту/кошелек/счет;
— Позволит записываться на групповые и персональные посещения;
— Поможет получить от клиента отзывы о визите к вам;
— Включает в себя сервис чаевых.
Для новых пользователей первый месяц бесплатно. Зарегистрироваться в сервисе
;
■ третичная структура (глобула) стабилизируется гидрофобными, ковалентными дисульфидными (-S-S-), ионными и водородными связями (эта структура характерна для многих бел ков-ферментов);
■ четвертичная структура — комплекс, образованный двумя, тремя, четырьмя и более белковыми молекулами, обладающими третичной структурой, за счет возникновения водородных, ионных и гидрофобных связей между ними; характерна для высокоспециализированных белков (пример — гемоглобин).
❖ Простые и сложные белки:
■ в состав простых белков (протеинов) входят только аминокислоты; к ним относятся многие ферменты;
■ сложные белки (протеиды) — белки, содержащие, помимо аминокислот, нуклеиновые кислоты (нуклеопротеиды), липиды (липопротеиды), углеводы (гликопротенды) и др.
❖ Основные свойства белков: гидрофильность (водорасгво-римость), видовая специфичность, химическая активность, способность денатурировать и ре натур ировать, изменять конфигурацию молекул под действием факторов среды.
Денатурация белка — утрата белковой молекулой своей структурной организации при воздействии химических веществ (кислот, щелочей, спиртов, солей и т.д.) и/или физических факторов (высокой температуры и/или давления, ионизирующих излучений и др.) вследствие разрушения водородных и ионных связей, поддерживающих вторичную, третичную и четвертичную структуры белка.
Ренатурация белка — процесс восстановления структуры белка после прекращения действия денатурирующего фактора, если его действие не привело к нарушению первичной структуры белка.
❖ Функции белков:
■ структурная, или строительная (входят в состав клеточных мембран, хрящей, сухожилий, волос, когтей, перьев и т.д.);
■ каталитическая, или ферментативная (ускоряют протекание химических реакций в клетке);
■ транспортная (участвуют в транспорте веществ через клеточные мембраны, ряд белков присоединяет и переносит с потоками крови различные вещества по организму);
■ двигательная (являются прямыми участниками механизма сокращения мышц и внутриклеточных сокращений);
■ защитная (входят в состав кожи позвоночных и антител, связывающих инородные белки; участвуют в свертывании крови при кровотечениях и т.д.);
■ запасающая (некоторые белки запасают необходимые организму вещества; например, миоглобин содержит запас кислорода в мышцах позвоночных);
■ энергетическая (служат источником энергии: I г дает 17,6 кДж);
■регуляторная (белки-гормоны поддерживают постоянные концентрации веществ в клетках и в крови, участвуют в обеспечении роста, размножения и других процессов);
■ сигнальная, или рецепторная (ответственны за распознавание «своих» и «чужих» клеток, являются важнейшей составной частью рецепторов).
❖ Примеры белков: актин я миозин (основные компоненты волокон поперечнополосатых мышц), гемоглобин (переносит кислород и углекислый газ), кератин (структурный белок волос, когтей, перьев, рогов), эластин (эластичный компонент соединительной ткани связок, стенок кровеносных сосудов), коллаген (компонент кожи и соединительной ткани костей, хрящей и сухожилий), амилаза (превращает крахмал в глюкозу) и др.
Ферменты (энзимы)
Ферменты (или энзимы) — это имеющие белковую природу биологические катализаторы, т.е. избирательно действующие органические вещества, в тысячи раз (при температуре порядка 37^10 °С) ускоряющие протекание биохимических реакций в клетке.
■ Многие ферменты находятся на мембранах клеток, митохондрий и т.д. и участвуют в транспорте веществ.
❖ Структура ферментов. Молекулы ферментов содержат:
■ белковый компонент (апоферменг);
■ сложное небелковое органическое соединение (кофермент) -только у двухкомпонентных ферментов, или ионы металлов (кофактор);
■ активный центр (один или несколько) — функциональная группа (например, -ОН), отдельная аминокислота или кофермент, обеспечивающие специфичность действия фермента за счет тесного, многоточечного контакта между молекулой фермента и определенного специфического вещества (субстрата);
■ регуляторный центр (один или несколько; у некоторых ферментов), с которым могут связываться молекулы-модуляторы или ингибиторы, регулирующие (модуляторы) или подавляющие (ингибиторы) активность фермента.
❖ Свойства ферментов:
■ специфичность (каждый фермент катализирует только те реакции, в которых участвуют молекулы лишь какого-нибудь одного или нескольких видов);
■ активность только в определенном интервале температур
(обычно не выше 50 -60 °С , редко до 80-90 °С );
■ для каждого фермента существует свое оптимальное значение pH, при котором этот фермент наиболее активен.
❖ Основные классы ферментов:
■ синтетазы (или лигазы) — катализируют реакции соединения молекул с образованием новых связей С-О, C-S, C-N, С-С {примеры. АТФ-синтетаза, ДНК-полимераза и др.);
■ гидролазы — катализируют реакции расщепления сложных органических веществ до простых путем присоединения молекул воды в месте разрыва химической связи в исходной молекуле (примеры: нуклеазы, расщепляющие нуклеиновые кислоты; амилазы, липазы);
■ изомераты — катализируют превращение одного изомера органического соединения в другой (пример: ДНК-топаизомераза);
■ лиазы — катализируют негидролитическое присоединение к субстрату или отщепление от него группы атомов (пример: декарбоксилаза);
■оксидоредуктазы — катализируют окислительно-восстановительные реакции, осуществляя перенос атомов Н и О или электронов от одного вещества к другому (примеры: ферменты цикла Кребса, тканевого дыхания);
■ трансферазы — катализируют перенос группы атомов (метиль-ной, ацильной, фосфатной или аминогруппы) от одного вещества к другому (пример: фосфотрансфераза).
Липиды
❖ Липиды — жироподобные органические соединения, представляющие собой сложные эфиры высших карбоновых кислот и трехатомного спирта глицерина или других спиртов.
■ В большинстве клеток содержится от 5 до 15% (по массе сухого вещества) липидов, в клетках подкожной жировой клетчатки — до 90%.
❖ Важнейшие классы липидов:
■ триацилглицеролы (твердые жиры и жидкие масла);
■ фосфолипиды;
■ гликолипиды;
■ терпены (ростовые вещества растений);
■ воски;
■ стероиды.
❖ Основные свойства липидов:
■ из всех биомолекул имеют наименьшую молекулярную массу;
■ в молекулах почти полностью отсутствуют полярные группы;
■ гидрофобны (нерастворимы в воде), но хорошо растворяются в органических растворителях (эфире, бензине, хлороформе);
■ могут образовывать сложные комплексы с белками (липопротеины), углеводами (гликолипиды), остатками фосфорной кислоты (фосфолипиды) и др.
Функции липидов:
■ структурная, или строительная (фосфолипиды, гликолипиды и липопротеины входят в состав клеточных мембран);
■ энергетическая (служат источником энергии: I г дает 38,9 кДж);
■ запасающая (большая часть энергетических запасов организма хранится в форме липидов);
■ защитная (подкожный и окружающий некоторые органы жировой слой является защитой от механических повреждений; подкожный жир предохраняет от потерь тепла и т.д.);
■ смазывающая и водоотталкивающая (воски покрывают кожу, шерсть, перья);
■ регуляторная (многие гормоны являются производными липоида холестерона, многие липиды — компоненты витаминов)-,
■ метаболическая (липиды — источник метаболической воды).
Углеводы (сахариды)
Углеводы — это вещества с общей формулой Си(Н20)„„ где п и ш некоторые целые числа.
■ Углеводороды образуются из неорганических веществ (Н20) и С02) в процессе фотосинтеза, происходящего в хлоропла-стах зеленых растений; являются исходными продуктами биосинтеза других органических веществ в растениях.
■ Содержание углеводов: в растительной клетке — до 85-90% сухого вещества, в животной клетке — примерно 1-2%.
Классификация углеводов. Углеводы делятся на:
■ моносахариды (или простые сахара), содержащие от 3 (три-озы) до 7 (гептозы) атомов углерода: рибоза, дезоксирибоза (пентозы), глюкоза, фруктоза (гексозы) и др.; они сладкие на вкус, хорошо растворимы в воде, молекулы моносахаридов -альдегидо- или кетоспирты;
■ олигосахариды (содержат от 2 до 10 моносахаридных остатков, соединенных гликозидными — через атом кислорода -связями): мальтоза, лактоза, сахароза и др.; имеют сладкий вкус, хорошо растворимы в воде;
■ полисахариды (высокомолекулярные сахара): целлюлоза, крахмал, гликоген, хитин и др.; они не имеют сладкого вкуса и нерастворимы в воде.
❖ Функции углеводов:
■ энергетическая (глюкоза — главный источник энергии в клетке); при расщеплении 1 г углевода освобождается 17,6 кДж энергии;
■ запасающая (часть энергетических запасов клеток хранится в форме крахмала или гликогена);
■ структурная, или строительная, и защитная (целлюлоза, хитин);
■ метаболическая (моносахариды — исходный продукт для синтеза многих органических веществ клетки).
Рибоза и дезоксирибоза — пятиуглеродные углеводы (простые сахара), являющиеся составными частями нуклеотидов молекул РНК (рибоза), ДНК (дезоксирибоза) и АТФ (рибоза); в свободном виде не встречаются.
Глюкоза — моносахарид с 6 атомами углерода, чрезвычайно широко распространенный в природе и являющийся первичным источником энергии в клетке; у растений образуется в результате фотосинтеза; в свободном виде содержится в плодах и цветках растений, в крови, лимфе, тканях мозга; входит в состав сахарозы, лактозы, гликогена, крахмала, целлюлозы и др.
Гликоген — полисахарид, состоящий примерно из 30 000 остатков глюкозы; содержится в грибах и тканях животных и человека (накапливается в печени и мышцах); участвует в углеродном обмене, является поставщиком глюкозы в кровь.
Крахмал — смесь двух полисахаридов — амилозы и амилопек-тина; один из важнейших полимеров глюкозы.
Целлюлоза — углевод, образующийся в растениях в результате полимеризации глюкозы; обладает высокой прочностью, не растворяется в воде, является одним из важнейших компонентов клеточных стенок. Используется для производства бумаги, вискозного шелка, различных тканей.
Хитин — полисахарид, являющийся основным компонентом наружного покрова членистоногих и входящий в состав клеточных стенок некоторых протистов и грибов; плохо растворим в воде.
Гепарин — гликопротеин, препятствующий свертыванию крови в кровеносных сосудах и участвующий в регуляции обмена липидов и иммунных реакциях организма.
Пигменты
❖ Пигменты — это окрашенные соединения в составе раститель-
ных и животных клеток; вещества, избирательно поглощающие свет определенных диапазонов видимой области спектра.
■ Пигменты являются сложными эфирами хлорофиллиновой кислоты и спиртов (фитола и метанола).
■ Представители пигментов: хлорофиллы a, b, с, d (участвуют в фотосинтезе), ксантофиллы (содержат атомы кислорода), каротины (не содержат атомов кислорода).
■ Пигменты входят в состав различных ферментов, включаются в структуру клеточных мембран.
❖ Функции пигментов:
■ обеспечивают фотосинтез (хлорофиллы);
■ придают окраску организмам;
■ участвуют в дыхании (гемоглобин);
■ играют важную роль в зрении (родопсины);
* защищают организм от ультрафиолетового излучения (у растений — каротиноиды, у животных — меланин).